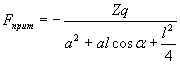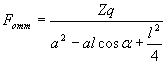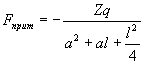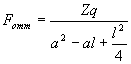|
ТЕОРИЯ СТРОЕНИЯ КООРДИНАЦИОННЫХ СОЕДИНЕНИЙ Курс лекций для студентов химфака ЮФУ (РГУ) ПРИРОДА СИЛ КОМПЛЕКСООБРАЗОВАНИЯ О природе сил комплексообразования – Электростатические представления – Энергия комплексного иона – Критерий Ламберта – Ион-дипольное взаимодействие Ион-дипольное взаимодействие Коссель – применил простые электростатические представления для расчета существования комплексов с ацидолигандами. Магнус с успехом распространил те же представления на комплексы с полярными молекулами типа H2O, NH3, C5H5N и т.д. Рассчитаем силу и энергию ион-дипольного взаимодействия. Диполь величиной µ = ql расположен на расстоянии
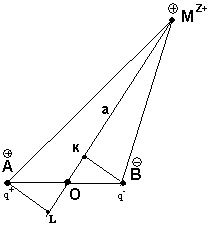
|MO| = а от металла, несущего заряд «+Z». Диполь ориентирован так, что отрицательный полюс расположен ближе к положительно заряженному иону металла, причем направлен по отношению к координационной связи
|OM| под углом
Найдем значения сил отталкивания и притяжения, используя закон Кулона.
Расстояние |OB| = |OA| = l/2 Треугольник ВОК – прямоугольный, тогда |BM|2 = |KB|2 + |KM|2 = |KB|2 + (a - |KO|)2 |KB| = |OB| |KO|= |OB| |BM|2 = |KB|2 + (a - |KO|)2 = Отсюда получаем
Аналогично можно найти и силу отталкивания Fотт.
Эти точные выражение, но их можно упростить. 1. Примем, что ось диполя совпадает с направлением ОM (или прямой а). Это наблюдается в действительности при отсутствии теплового движение, т.е. при 0 К. Но при высоких температурах всегда имеется часть молекул, ориентированная под углом 0. Ошибка зависит от величины дипольного момента молекулы лиганда. Так как cos α = cos 0° = 1, то
2. В выражении для дипольного момента l – расстояние между центрами тяжести зарядов диполя; оно значительно меньше расстояния от центра диполя до металла М. Поэтому l ‹ a и Теперь можно найти сумму сил в данном комплексе: Fрез = После интегрирования можно найти энергию комплекса, как
|